Эверетт и борилазиды
Oct. 15th, 2015 11:34 pmКраткое содержание поста: История аспирантуры моего лабмейта Эверетта Мерлинга рассказывается параллельно с химией карбен-борилазидов (они же карбен-азидобораны). Смогут ли они вступить в реакцию [3+2]-циклоприсоединения с диполярофилами, а Эверетт защитить диссертацию?
***
Эверетт, мой приятель по лабе проф. Каррана, начал аспирантуру в Питтсбурге в 2009 году, через два года после меня. Сын двух врачей из Айовы, старший из 11 детей, eagle scout, кларнетист marching band в Xavier University в Цинциннати, владелец собственного дома в Питтсбурге (родители все же врачи) и разрешения на ношение оружия оказался республиканцем, неплохим химиком и несколько инфантильным интеллигентом в очках.
Назначен он был на тот же карбен-борановый проект, по которому уже успешно работал я и несколько постдоков. Профессор предложил ему поиграть с карбен-борилазидами NHC-BH2N3. Азиды RN3 - интересные звери сами по себе. Азид натрия используется в подушках безопасности, азид свинца - в детонаторах, и все мы ждем Нобеля за клик-химию, где реакция азидов с алкинами является самым ярким примером. А вот я приготовил карбен-борилазид.

Это не был самый первый борилазид вообще, но первый стабильный, который можно на колонке почистить и в баночку положить. Немецкие химики еще задолго до Thomas Klapötke в 1960-е годы любили приготовить и жахнуть какой-нибудь B(N3)3. Но я честно не собирался ничего взрывать. Для меня это в первую очередь был “еще один нуклеофил”, с которым можно было провести реакцию замещения на атоме бора, насинтезировать необычных веществ, получить их X-ray структуры и опубликовать свою главную статью в JACS’е.
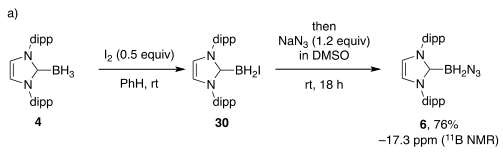
Однако потенциальную взрывоопасность мы не игнорировали. Наш французский коллаборатор Эммануэль предлагал связаться с ребятами, которые тестируют взрывчатые вещества на стабильность, ударяя по ним молотком. Но Карран приобрел для лабы книжку по химии азидов, где в первой главе мы вычитали об эмпирическом правиле: если в веществе количество азотов в 3 и более раз меньше, чем остальных тяжелых элементов (то есть без водородов), то можно работать и не бояться, что оно взорвется: (C + B + O) / N ≥ 3. Для моих больших и рогатых карбенов формула азида получалась C27H38BN5, (27 + 1) / 5 = 5,6. Он плавился без разложения при 180-182 ºC. Пузырьки газа начинали выделяться только выше 270 ºC. Проблемой станет, наоборот, заставить его хоть как-то прореагировать дальше.
Люблю я такие стабильные соединения. Вот Эверетт попробовал получить борилазид с наименьшим карбеном, где вместо рогатых групп метилы, и, конечно, выделить его не смог. Хранил в растворе в морозилке. Для C5H12BN5 правило дает (5 + 1) / 5 = 1,2 - потенциально взрывоопасно. Более того, в ЯМР Эверетт наблюдал сигнал от карбен-триазидоборана NHC-B(N3)3 и благоразумно отметил: “The triazide 84 has an extremely low carbon-to-nitrogen ratio of 0.45, so we did not pursue isolation of this compound”.
А вот я с большим карбеном готовил диазид, выделял, кристаллизовал и не боялся, так как там соотношение 3,5. Я вообще-то к технике безопасности очень строго стал относиться за время аспирантуры. Взрывы у нас в лабе были, но не с азидами, а с перхлоратами. Недаром и в своей группе Хартвиг просил, чтобы перед работой с азидами и перхлоратами все получали его персональное благословение. А я понял, что самое главное даже не химическая природа вещества, а его количество - scale. Если работать с 40 мг, то ничего плохого не случится.
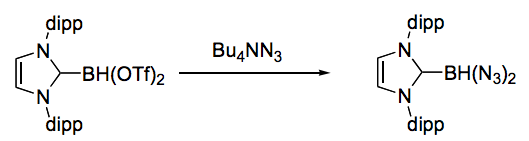
Может быть, именно потому, что для меня карбен-борилазид был всего лишь еще одним необычным веществом, подпроектом подпроекта, самую красивую реакцию с ним суждено было провести не мне - первооткрывателю, а новичку Эверетту. Я, конечно, знал химию органических азидов и видел четкие параллели между карбен-боранами и углеводородами, но выписав список идей, что можно дальше сделать с моим азидом, зациклился на его восстановлении.
Получение NHC-BH2NH2 стало моей идеей-фикс, но я так и не синтезировал его ни одним из многочисленных способов. Обыкновенные азиды можно восстановить боранами, но я уже знал, что B-H связи в карбен-боранах для этой цели дубовые, а потому две эти функциональные группы мирно сосуществуют. Ни LiAlH4, ни Ph3P, ни H2, Pd/C, которые бы со свистом восстановили алкил- или арилазиды, не брали NHC-BH2N3. С веществом ничего не происходило. Уж не знаю, виной тому стерические или электронные эффекты, или все вместе, но я обиделся на азиды и переключился на другие проекты.
И тогда Карран на очередном сабгрупп-митинге карбен-боранщиков предложил Эверетту попробовать [3+2]-циклоприсоединение карбен-борилазида с алкинами. А андеграду Владимиру - ту же реакцию с нитрилами. Так NHC-BH2N3 перестал быть “моим азидом” и стал нашим.
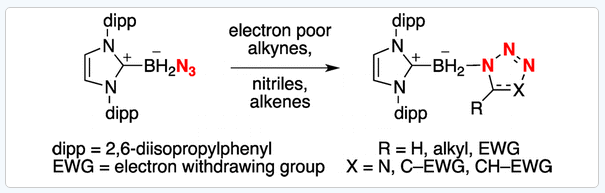
Владимир - тоже интересный персонаж. Кажется, химия была у него minor, а major он был в социологии. Или наоборот. Но неважно. Он даже немного говорил по-русски (приехал в США в детстве с родителями и братом-близнецом Николаем) и был несколько медлителен. Я даже разозлился на него однажды, когда он перепутал иод и азид натрия. Ну, прямо черное с белым. Да, учить Владимира химическим премудростям назначили именно меня. В целом, карбен-бораны - прекрасный обучающий проект. Начинается с довольно простого, но поучительного трехстадийного синтеза NHC-BH3, а там уже недалеко (one-pot - “один горшок”) до NHC-BH2N3.
Но постепенно Владимир выучился и синтезу, и колоночной хроматографии, и снятию спектров ЯМР (хотя долго таскал с собой шпаргалку с командами для компьютера), и даже начал генерить собственные идеи, с чем еще можно ввести в реакцию азид. После получения бакалавра он остался в группе Каррана мастер-стьюдентом, но как только его приняли в медшколу, свалил из химии, как и другой наш андеград Джордан.
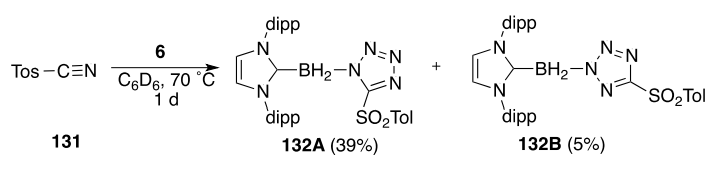
Итак, задача руководством была поставлена ясная: сочетать борилазид с любым нитрилом в борилтетразол. “The reaction with acetonitrile should be fast enough even at room temperature”, - сказал Карран. Авотфиг. И с бензонитрилом фиг. Четырехкоординированный бор делает азид настолько электронодонорным, что нужен был электронакцепторный нитрил. Я посмотрел по базе реактивов, что у нас имеется в наличии. Во, тозилцианид - 4-MeC6H4S(=O)2CN - если и с этим не получится, то дохлое дело. При умеренном нагревании тозилцианид и карбен-борилазид сочетались двумя ковалентыми связями и дали здоровые, разделяемые на колонке тетразолы.
А Эверетт тем временем химичил с алкинами. И пришел к тем же выводам, что алкин должен быть электронакцепторным: например, пропиолатом или даже ацетилендикарбоксилатом. С неактивированными алкинами реакция шла медленно. Я помню, как заходил к Эверетту в лабу, и у него в тяге днями грелись ЯМР ампулы, но и 10 дней в толуоле при 110 ºС подчас не хватало, чтобы весь азид прореагировал. Микроволновка или катализ медными солями помогали мало, если вообще помогали.
Региоселективность, конечно, была большим вопросом. С монозамещенными алкинами обычно получались 1,4-замещенные триазолы, с нитрилами - 1,5-замещенные тетразолы, с дизамещенными алкинами - смеси 1,4- и 1,5-триазолов. Это, конечно, все было подтверждено X-ray структурами. Я тогда умел на пальцах объяснить, почему получается именно так. Но через 3 года китайцы-теоретики эти наши реакции обсчитали и сказали, что все так и должно быть. Но я в орбитали не верю. Верю в синтез, ЯМР и рентген.
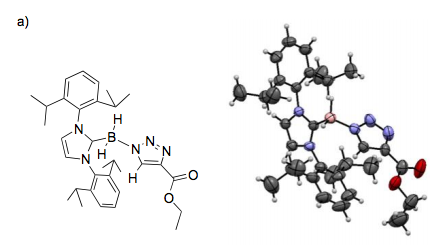
Пришла пора писать статью, которая вышла в Org. Lett. в 2012 году. Эверетт был первым автором, Владимир вторым, я даже не попал в Acknowledgment и вообще уже был в Берклях, но все равно чувствовал сопричастность к этой работе. Красивая все же реакция. Вы только посмотрите на эти аддукты - тут же и связь с другой большой темой в группе Каррана - fluorous chemistry:
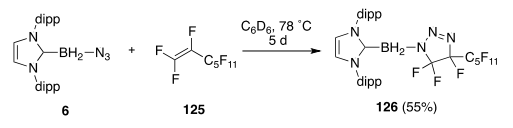
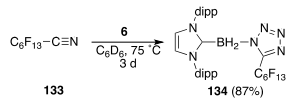
Недаром на конференциях по моему постеру вопросов о карбен-борилазидах было всегда больше всего. А когда я рассказал одному профессору из Северной Каролины о том, что мы их научились [3+2]-циклоприсоединять, ему это ужасно понравилось. Он сам циклоприсоединял сульфонилазиды. Это вообще стало модным, целое направление: сочетать X-N3 c диполярофилами, перебирая все X в периодической системе: от бора до молибдена. Но с борилазидами наша группа была первой. Потом уже подключились остальные, включая мощного неорганика Дугласа Стефана из Торонто, и эта статья Эверетта накопила за 3 года 20 штук цитирований.
Но в этот момент Эверетт и карбен-борилазиды зашли в творческий тупик. Я защитился в декабре 2011 года. Эверетт в тот момент безуспешно пытался что-то сделать дальше с продуктами циклоприсоединения, отделить карбен-борильную часть и преподнести это как новый способ синтеза триазолов. Но карбен-бораны иногда настолько упрямы, что их не возьмешь концентрированной кислотой. Эверетту пришлось довольствоваться сомнительными результатами, которые в статью было решено не включать.
В том же 2012 году у него вышла вторая статья в Org. Lett. - коллаборейшн с немецкой группой Herbert Mayr по количественной оценке нуклеофильности NHC-BH3 и их присоединению к некоторым электронакцепторным алкенам (но это тема для отдельного поста). И все. Больше за годы аспирантуры статей Эверетт не опубликовал.
У меня стоят Google Scholar alerts на все статьи из группы Каррана и все статьи по карбен-боранам. Я следил, как публиковались и защитились по этой теме два других аспиранта. Как канадцы использовали наш карбен-борилазид для синтеза ”неорганического ацетилена HBNH”, а статей Эверетта больше не появлялось.
Год назад я написал ему в числе нескольких моих знакомых, чтобы рассказать о своем пути из постдоков в мобильные разработчики. Он быстро ответил, поздравил меня, но признался, что подзадержался в группе Каррана, после защиты своего classmate Бена стал в группе самым старшим - необычное чувство. Что он потратил 8 месяцев на придумывание original proposal’а - обязательное требование для защиты. Что, откровенно говоря, химия ему надоела, но защищаться надо, профессор Карран хочет, чтобы он закончил до конца 2014 года. В своем последнем письме в декабре он все еще писал диссер.
Наконец, на прошлой неделе я получил Google Alert на его диссертацию, которая была защищена в конце апреля, а в конце сентября стала доступна для скачивания на сайте Университета Питтсбурга. Вечер понедельника я провел за чтением и химическими воспоминаниями. Хотя полностью новых вещей в диссертации было неожиданно мало. Все это была химия, которую мы 4 года назад обсуждали на сабгруппах. 80% диссера Эверетт сделал за один год: с осени 2010-го по осень 2011 года. Экспериментальная часть почти полностью скопирована из тех двух статей. Даже результаты Владимира включены с пометкой “cycloadditions of nitriles and select alkenes were tested with the help of an undergraduate worker Mr. V. Lamm”, что для меня выглядит натянуто - экспериментально это все было сделано Владимиром без участия Эверетта.
У меня диссер был на 250 страниц с 96 новыми охарактеризованными карбен-боранами (я считаю по HRMS). У Эверетта - 120 страниц и 22 новых вещества (с многочисленными ляпами в экспериментальной части, когда данные по одному соединению оказываются под другим или вообще исчезают). Все же повезло ему, что вначале попалась работающая реакция, которая позволила потом работать, не боясь, что не на чем будет защищаться. Или не повезло? И, наоборот, сбило не на тот путь и лишило мотивации?
После чтения диссертации мне сложно представить, чем он занимался последующие 3,5 года: от моей защиты до своей. Ну, готовил пропозал, писал диссер - пусть это год. Классов и преподавания у него уже не оставалось. Те неудачные реакции, которые у него там описаны, но опубликованы не были - это тоже год с самой большой натяжкой. Одна из его проблем в том, что я в основном работал с массивными карбенами, с рогатыми заместителями, а Эверетт - с простейшим 1,3-диметилимидазолиденом. Последний дешевле синтезировать, и у diMe-Imd-BH3 минимальные стерические трудности. Потому он хорош, как реагент, но если надо выделить и охарактеризовать карбен-борановый продукт, то лучше идти по моему пути. Эверетт пытался его повторить с меньшим карбеном (зачем?) и постоянно натыкался на быстро разлагающиеся продукты, которые можно было только заметить в 11B ЯМР и то чаще в виде смеси.
Свой профиль на linkedin Эверетт не обновлял, оставаясь вечным аспирантом. Но там я нашел его не @pitt.edu адрес и написал запоздалое поздравление с получением PhD и о том, что я прочитал его диссертацию.
Он мне быстро ответил. Пошутил, что теперь он не единственный человек, который читал его диссертацию. Рассказал, что продал дом в Питтсбурге, вернулся к родителям и рассекает на мотоциклах с младшими братьями по Мидвесту - роскошь, которую могут себе позволить американские выпускники, потому что им не нужно думать об иммиграционном статусе. Пробовал он преподавать органическую химию в маленьком колледже, но через пару месяцев бросил - не его. Будет искать работу в химической индустрии в Цинциннати. Почему именно в Цинциннати, я его не спросил.
***
Эверетт, мой приятель по лабе проф. Каррана, начал аспирантуру в Питтсбурге в 2009 году, через два года после меня. Сын двух врачей из Айовы, старший из 11 детей, eagle scout, кларнетист marching band в Xavier University в Цинциннати, владелец собственного дома в Питтсбурге (родители все же врачи) и разрешения на ношение оружия оказался республиканцем, неплохим химиком и несколько инфантильным интеллигентом в очках.
Назначен он был на тот же карбен-борановый проект, по которому уже успешно работал я и несколько постдоков. Профессор предложил ему поиграть с карбен-борилазидами NHC-BH2N3. Азиды RN3 - интересные звери сами по себе. Азид натрия используется в подушках безопасности, азид свинца - в детонаторах, и все мы ждем Нобеля за клик-химию, где реакция азидов с алкинами является самым ярким примером. А вот я приготовил карбен-борилазид.

Это не был самый первый борилазид вообще, но первый стабильный, который можно на колонке почистить и в баночку положить. Немецкие химики еще задолго до Thomas Klapötke в 1960-е годы любили приготовить и жахнуть какой-нибудь B(N3)3. Но я честно не собирался ничего взрывать. Для меня это в первую очередь был “еще один нуклеофил”, с которым можно было провести реакцию замещения на атоме бора, насинтезировать необычных веществ, получить их X-ray структуры и опубликовать свою главную статью в JACS’е.

Однако потенциальную взрывоопасность мы не игнорировали. Наш французский коллаборатор Эммануэль предлагал связаться с ребятами, которые тестируют взрывчатые вещества на стабильность, ударяя по ним молотком. Но Карран приобрел для лабы книжку по химии азидов, где в первой главе мы вычитали об эмпирическом правиле: если в веществе количество азотов в 3 и более раз меньше, чем остальных тяжелых элементов (то есть без водородов), то можно работать и не бояться, что оно взорвется: (C + B + O) / N ≥ 3. Для моих больших и рогатых карбенов формула азида получалась C27H38BN5, (27 + 1) / 5 = 5,6. Он плавился без разложения при 180-182 ºC. Пузырьки газа начинали выделяться только выше 270 ºC. Проблемой станет, наоборот, заставить его хоть как-то прореагировать дальше.
Люблю я такие стабильные соединения. Вот Эверетт попробовал получить борилазид с наименьшим карбеном, где вместо рогатых групп метилы, и, конечно, выделить его не смог. Хранил в растворе в морозилке. Для C5H12BN5 правило дает (5 + 1) / 5 = 1,2 - потенциально взрывоопасно. Более того, в ЯМР Эверетт наблюдал сигнал от карбен-триазидоборана NHC-B(N3)3 и благоразумно отметил: “The triazide 84 has an extremely low carbon-to-nitrogen ratio of 0.45, so we did not pursue isolation of this compound”.
А вот я с большим карбеном готовил диазид, выделял, кристаллизовал и не боялся, так как там соотношение 3,5. Я вообще-то к технике безопасности очень строго стал относиться за время аспирантуры. Взрывы у нас в лабе были, но не с азидами, а с перхлоратами. Недаром и в своей группе Хартвиг просил, чтобы перед работой с азидами и перхлоратами все получали его персональное благословение. А я понял, что самое главное даже не химическая природа вещества, а его количество - scale. Если работать с 40 мг, то ничего плохого не случится.

Может быть, именно потому, что для меня карбен-борилазид был всего лишь еще одним необычным веществом, подпроектом подпроекта, самую красивую реакцию с ним суждено было провести не мне - первооткрывателю, а новичку Эверетту. Я, конечно, знал химию органических азидов и видел четкие параллели между карбен-боранами и углеводородами, но выписав список идей, что можно дальше сделать с моим азидом, зациклился на его восстановлении.
Получение NHC-BH2NH2 стало моей идеей-фикс, но я так и не синтезировал его ни одним из многочисленных способов. Обыкновенные азиды можно восстановить боранами, но я уже знал, что B-H связи в карбен-боранах для этой цели дубовые, а потому две эти функциональные группы мирно сосуществуют. Ни LiAlH4, ни Ph3P, ни H2, Pd/C, которые бы со свистом восстановили алкил- или арилазиды, не брали NHC-BH2N3. С веществом ничего не происходило. Уж не знаю, виной тому стерические или электронные эффекты, или все вместе, но я обиделся на азиды и переключился на другие проекты.
И тогда Карран на очередном сабгрупп-митинге карбен-боранщиков предложил Эверетту попробовать [3+2]-циклоприсоединение карбен-борилазида с алкинами. А андеграду Владимиру - ту же реакцию с нитрилами. Так NHC-BH2N3 перестал быть “моим азидом” и стал нашим.

Владимир - тоже интересный персонаж. Кажется, химия была у него minor, а major он был в социологии. Или наоборот. Но неважно. Он даже немного говорил по-русски (приехал в США в детстве с родителями и братом-близнецом Николаем) и был несколько медлителен. Я даже разозлился на него однажды, когда он перепутал иод и азид натрия. Ну, прямо черное с белым. Да, учить Владимира химическим премудростям назначили именно меня. В целом, карбен-бораны - прекрасный обучающий проект. Начинается с довольно простого, но поучительного трехстадийного синтеза NHC-BH3, а там уже недалеко (one-pot - “один горшок”) до NHC-BH2N3.
Но постепенно Владимир выучился и синтезу, и колоночной хроматографии, и снятию спектров ЯМР (хотя долго таскал с собой шпаргалку с командами для компьютера), и даже начал генерить собственные идеи, с чем еще можно ввести в реакцию азид. После получения бакалавра он остался в группе Каррана мастер-стьюдентом, но как только его приняли в медшколу, свалил из химии, как и другой наш андеград Джордан.
Итак, задача руководством была поставлена ясная: сочетать борилазид с любым нитрилом в борилтетразол. “The reaction with acetonitrile should be fast enough even at room temperature”, - сказал Карран. Авотфиг. И с бензонитрилом фиг. Четырехкоординированный бор делает азид настолько электронодонорным, что нужен был электронакцепторный нитрил. Я посмотрел по базе реактивов, что у нас имеется в наличии. Во, тозилцианид - 4-MeC6H4S(=O)2CN - если и с этим не получится, то дохлое дело. При умеренном нагревании тозилцианид и карбен-борилазид сочетались двумя ковалентыми связями и дали здоровые, разделяемые на колонке тетразолы.

А Эверетт тем временем химичил с алкинами. И пришел к тем же выводам, что алкин должен быть электронакцепторным: например, пропиолатом или даже ацетилендикарбоксилатом. С неактивированными алкинами реакция шла медленно. Я помню, как заходил к Эверетту в лабу, и у него в тяге днями грелись ЯМР ампулы, но и 10 дней в толуоле при 110 ºС подчас не хватало, чтобы весь азид прореагировал. Микроволновка или катализ медными солями помогали мало, если вообще помогали.
Региоселективность, конечно, была большим вопросом. С монозамещенными алкинами обычно получались 1,4-замещенные триазолы, с нитрилами - 1,5-замещенные тетразолы, с дизамещенными алкинами - смеси 1,4- и 1,5-триазолов. Это, конечно, все было подтверждено X-ray структурами. Я тогда умел на пальцах объяснить, почему получается именно так. Но через 3 года китайцы-теоретики эти наши реакции обсчитали и сказали, что все так и должно быть. Но я в орбитали не верю. Верю в синтез, ЯМР и рентген.

Пришла пора писать статью, которая вышла в Org. Lett. в 2012 году. Эверетт был первым автором, Владимир вторым, я даже не попал в Acknowledgment и вообще уже был в Берклях, но все равно чувствовал сопричастность к этой работе. Красивая все же реакция. Вы только посмотрите на эти аддукты - тут же и связь с другой большой темой в группе Каррана - fluorous chemistry:


Недаром на конференциях по моему постеру вопросов о карбен-борилазидах было всегда больше всего. А когда я рассказал одному профессору из Северной Каролины о том, что мы их научились [3+2]-циклоприсоединять, ему это ужасно понравилось. Он сам циклоприсоединял сульфонилазиды. Это вообще стало модным, целое направление: сочетать X-N3 c диполярофилами, перебирая все X в периодической системе: от бора до молибдена. Но с борилазидами наша группа была первой. Потом уже подключились остальные, включая мощного неорганика Дугласа Стефана из Торонто, и эта статья Эверетта накопила за 3 года 20 штук цитирований.
Но в этот момент Эверетт и карбен-борилазиды зашли в творческий тупик. Я защитился в декабре 2011 года. Эверетт в тот момент безуспешно пытался что-то сделать дальше с продуктами циклоприсоединения, отделить карбен-борильную часть и преподнести это как новый способ синтеза триазолов. Но карбен-бораны иногда настолько упрямы, что их не возьмешь концентрированной кислотой. Эверетту пришлось довольствоваться сомнительными результатами, которые в статью было решено не включать.
В том же 2012 году у него вышла вторая статья в Org. Lett. - коллаборейшн с немецкой группой Herbert Mayr по количественной оценке нуклеофильности NHC-BH3 и их присоединению к некоторым электронакцепторным алкенам (но это тема для отдельного поста). И все. Больше за годы аспирантуры статей Эверетт не опубликовал.
У меня стоят Google Scholar alerts на все статьи из группы Каррана и все статьи по карбен-боранам. Я следил, как публиковались и защитились по этой теме два других аспиранта. Как канадцы использовали наш карбен-борилазид для синтеза ”неорганического ацетилена HBNH”, а статей Эверетта больше не появлялось.
Год назад я написал ему в числе нескольких моих знакомых, чтобы рассказать о своем пути из постдоков в мобильные разработчики. Он быстро ответил, поздравил меня, но признался, что подзадержался в группе Каррана, после защиты своего classmate Бена стал в группе самым старшим - необычное чувство. Что он потратил 8 месяцев на придумывание original proposal’а - обязательное требование для защиты. Что, откровенно говоря, химия ему надоела, но защищаться надо, профессор Карран хочет, чтобы он закончил до конца 2014 года. В своем последнем письме в декабре он все еще писал диссер.
Наконец, на прошлой неделе я получил Google Alert на его диссертацию, которая была защищена в конце апреля, а в конце сентября стала доступна для скачивания на сайте Университета Питтсбурга. Вечер понедельника я провел за чтением и химическими воспоминаниями. Хотя полностью новых вещей в диссертации было неожиданно мало. Все это была химия, которую мы 4 года назад обсуждали на сабгруппах. 80% диссера Эверетт сделал за один год: с осени 2010-го по осень 2011 года. Экспериментальная часть почти полностью скопирована из тех двух статей. Даже результаты Владимира включены с пометкой “cycloadditions of nitriles and select alkenes were tested with the help of an undergraduate worker Mr. V. Lamm”, что для меня выглядит натянуто - экспериментально это все было сделано Владимиром без участия Эверетта.
У меня диссер был на 250 страниц с 96 новыми охарактеризованными карбен-боранами (я считаю по HRMS). У Эверетта - 120 страниц и 22 новых вещества (с многочисленными ляпами в экспериментальной части, когда данные по одному соединению оказываются под другим или вообще исчезают). Все же повезло ему, что вначале попалась работающая реакция, которая позволила потом работать, не боясь, что не на чем будет защищаться. Или не повезло? И, наоборот, сбило не на тот путь и лишило мотивации?
После чтения диссертации мне сложно представить, чем он занимался последующие 3,5 года: от моей защиты до своей. Ну, готовил пропозал, писал диссер - пусть это год. Классов и преподавания у него уже не оставалось. Те неудачные реакции, которые у него там описаны, но опубликованы не были - это тоже год с самой большой натяжкой. Одна из его проблем в том, что я в основном работал с массивными карбенами, с рогатыми заместителями, а Эверетт - с простейшим 1,3-диметилимидазолиденом. Последний дешевле синтезировать, и у diMe-Imd-BH3 минимальные стерические трудности. Потому он хорош, как реагент, но если надо выделить и охарактеризовать карбен-борановый продукт, то лучше идти по моему пути. Эверетт пытался его повторить с меньшим карбеном (зачем?) и постоянно натыкался на быстро разлагающиеся продукты, которые можно было только заметить в 11B ЯМР и то чаще в виде смеси.
Свой профиль на linkedin Эверетт не обновлял, оставаясь вечным аспирантом. Но там я нашел его не @pitt.edu адрес и написал запоздалое поздравление с получением PhD и о том, что я прочитал его диссертацию.
Он мне быстро ответил. Пошутил, что теперь он не единственный человек, который читал его диссертацию. Рассказал, что продал дом в Питтсбурге, вернулся к родителям и рассекает на мотоциклах с младшими братьями по Мидвесту - роскошь, которую могут себе позволить американские выпускники, потому что им не нужно думать об иммиграционном статусе. Пробовал он преподавать органическую химию в маленьком колледже, но через пару месяцев бросил - не его. Будет искать работу в химической индустрии в Цинциннати. Почему именно в Цинциннати, я его не спросил.
no subject
Date: 2015-10-16 07:18 am (UTC)no subject
Date: 2015-10-16 07:28 am (UTC)У меня в планах постепенно рассказать обо всех своих химических публикациях. С годами обнаруживается возможность шире смотреть на многие вещи.
no subject
Date: 2015-10-16 10:44 am (UTC)no subject
Date: 2015-10-16 05:10 pm (UTC)no subject
Date: 2015-10-16 10:56 am (UTC)Жаль, конечно, что он ничего кроме 3+2 не нашел и не сделал. Такой маленький диссер в итоге получился...
Я бы, наверное, поискала бы какую-то замену дипп (особенно, раз это всего лишь трехстадийка), может нашлось бы что-нибудь еще более недорогое, стабилизирующее, но при этом позволяющее расширить границы изучения химии BN3. Например, замещенные индолы вместо фенила. Или наоборот, пиридины. Сварить небольшую таблицу зависимости заместителя от реакционной способности азида :). Может и для твоего восстановления в нашлось бы что-нибудь.
Интересно также (хотя я мало разбираюсь в химии бора): а реально ли вместо азида получить, например, что-то типа диазониевой соли? Тогда вообще можно было бы развернуться: триазены, замещения.
no subject
Date: 2015-10-16 05:25 pm (UTC)Диссер у Эверетта получился не самый маленький из тех, что я видел, но потенциал был сделать еще в 2-3 раза больше за то время, что он просидел в аспирантуре. Почему так получилось - для меня самого вопрос. Творческие кризисы в науке у всех случаются, и тогда надо вовремя переключаться на что-то новое. У меня всегда было полно идей по карбен-боранам, но за 3 года работы они меня так достали, что я хотел защититься как можно скорее.
Мы готовили карбен-бораны с более чем 20 разными карбенами. Мое мнение, что замена карбена ничего бы интересного в химию борилазидов не принесла. Они или большие, и тогда вся химия, как была у меня с dipp. Или маленькие, и тогда все разваливается. Но самое главное, я не вижу большого смысла сидеть с этими реакциями так долго. Эверетту нужно было придумывать что-то радикально новое. Пусть и бесполезное, вроде той ссылки на "неорганический ацетилен", где Эверетт всю химию мог проделать на 2 года раньше канадцев. Была бы статья первым автором в ACIE, плохо что ли? Но если бы он сварил такую таблицу борилазидов с разными карбенами, то мне хотя бы было понятно, чем он занимался, и у него был бы еще десяток новых веществ охарактеризован. Может, и нашел бы что-то необычное, достойное публикации.
Я верю, что получить карбен-борилдиазониевую соль можно: NHC-BH2N2+BF4-. Но я в литературе такого не видел. Карбен-аминоборан, который можно было бы попытаться диазотировать, я не получил. Нахимичить-то можно, но снова вопрос зачем? Если я вернусь когда-нибудь в экспериментальную химию, то постараюсь заняться более практическими вещами.
no subject
Date: 2015-10-17 05:56 am (UTC)А орбитали я и сама не уважаю, особенно когда народ начинает на них уж слишком налегать, рисовать кучу какой-то фигни и зуб давать, что там вот именно такая орбиталь именно вот так вот изогнулась в таком направлении и вообще как в этом сакральном знании кто-то может сомневаться. Больше всего в объяснении чего-то через орбитали меня смущает то, что это подгоняется под результат, что для такой казалось бы фундаментальной модели с несколькими якобы жутко логичными правилами должно без подгона работать, а вот нет - получился странный продукт, которого не ожидали - сейчас подгоним правильных орбиталей, чтобы все объяснить. Очень меня это смущает.
Забавно, моя вхкшная однокурсница у Майра получала дигри в группе ;-) Как же мир тесен в очередной раз.
no subject
Date: 2015-10-17 06:58 am (UTC)Мир становится действительно тесным, если учесть, что в то же время у Майра в группе был и мой однокурсник, который после получения ПхД отправился делать постдока к Хартвигу.
no subject
Date: 2015-11-05 05:46 am (UTC)На первом курсе апсирантуры я прочитал "Химию ацетиленовых соединений" (под ред. Вийе). Там мне рассказали, что двух пи-орбиталей в ацетилене НЕТ. А есть кольцеобразное осесимметричное облако. Ссылка на статью 1960-го емнип года.
С тех пор моя жизнь никогда уже не будет прежней :)
no subject
Date: 2015-10-17 06:39 am (UTC)Лайк за пост!:)
no subject
Date: 2015-10-17 07:00 am (UTC)Тут действительно хэппи-енд. Могло бы все сложиться намного печальнее, если бы ни одна реакция не сработала.
no subject
Date: 2015-10-17 11:24 am (UTC)Да, а когда медный катализ не работал, рутениевый не пытались использовать? Он тоже катализирует, но как раз в сторону другого изомера.
Написание original proposal - жёсткая штука. Мне вот за 5 лет в науке особо оригинальных идей не пришло. Разве что одна - крутить всякие сочетания на атоме фосфора или серы, используя их гипервалентность. Только исходные субстраты для таких сочетаний готовить надо с металлоорганикой и вообще геморройно, так что требуется доработка. Хм...пока писал, понял, что в принципе тут может помочь FLP.
http://research.chem.psu.edu/radosevichgrp/Research.html
Что-то вот в таком направлении.
А вообще, химия бора и фосфора - это круто!
Computational chemistry я сам не верю напрочь и рассматриваю её только как инструмент рисования красивых картинок для статьи. Эдакий Photoshop для химиков. В отличие от моего бывшего шефа, который придумал идею, рассчитал её и сказал, что "согласно расчётам, должно работать". Поставил туда Master student. Результат - его диплом был сугубо расчётный с ТОЛЬКО отрицательными экспериментальными результатами.
no subject
Date: 2015-10-17 05:11 pm (UTC)Насчет рутениевого катализа ничего в диссертации Эверетта я не увидел. Но у нашей реакции механизм определенной иной, чем у медь-катализируемого клика. Алкины вовсе не должны быть монозамещенными.
Original proposal и мне тяжело дался, но это уж моя проблема отсутствия хороших идей к концу аспирантуры. С химией бора и фосфора люди очень быстро сваливаются в оторванный от практики синтез экзотических соединений. Читать такие статьи иногда интересно, но заниматься этим всю жизнь я бы не хотел.
По нашему карбен-борановому проекту расчеты делались и в самом начале для скоростей радикального восстановления с помощью NHC-BH3 по сравнению с другими реагентами. Расчеты ошиблись на пару порядков, были забыты, выкинуты на помойку, и с расчетчиками больше Карран не пытался сотрудничать. Я даже горжусь, что в моих статьях нет расчетов. Иначе мне, наверняка, было бы за них стыдно, зная как мы их подгоняли под эксперимент. Расчеты имеют право на жизнь, но в узких, более физических, чем химических областях (в расчет хим. сдвигов в ЯМР я даже готов поверить), никак не для решения "пойдет ли реакция и в каком направлении".
no subject
Date: 2015-10-17 04:51 pm (UTC)По себе знаю.
no subject
Date: 2015-10-17 05:21 pm (UTC)Мое личное мнение я высказал: надо было понять, что Эверетту проект надоел, идей нет, и дать ему поработать над чем-нибудь другим. Хоть над полным синтезом. Часто такая смена проекта идет на пользу.
no subject
Date: 2015-10-19 10:13 am (UTC)Но это тык пальцем в небо - я лично никого из участников истории не знаю.
no subject
Date: 2015-10-17 05:08 pm (UTC)no subject
Date: 2015-10-17 05:31 pm (UTC)no subject
Date: 2015-10-17 06:20 pm (UTC)no subject
Date: 2015-10-17 06:32 pm (UTC)У химиков есть такая особенность, как Экспериментальная часть, где надо описать все проведенные эксперименты и аналитические данные по полученным веществам. У меня это 110 страниц. Читать это подряд никто в здравом уме не будет - это не текст для человеческого чтения. Там многое копипастится, так как вещества часто похожи, методы их получения похожи. Но для меня в органической химии именно размер экспериментальной части определяет то, сколько сделано по диссертации, реальный трудовой и научный вклад.
Еще 10 страниц - это библиография. 15 страниц - титульные листы, абстракт, оглавление, список сокращений. Остается 115 страниц - главная часть, но там так много схем, таблиц и рисунков, что я затрудняюсь сказать, сколько непосредственно текста буквами. Возможно, что те же 45 страниц. Но я, если и гнался, то за тем, чтобы уменьшить объем (мне же все это печатать в 4 экземплярах!). В частности я для членов своего коммитти раздавал еще диск с копиями моих статей и картинок ЯМР спектров, которые бы потянули еще на 150 страниц.
no subject
Date: 2015-10-17 06:48 pm (UTC)no subject
Date: 2015-10-17 07:12 pm (UTC)